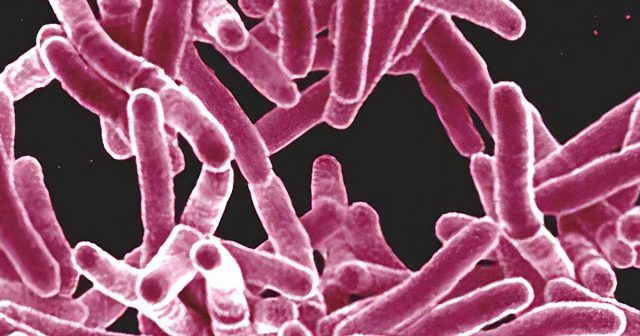
Causada por la bacteria Mycobacterium tuberculosis, la tuberculosis afecta a un tercio de la población mundial y ocasiona alrededor de 1,8 millones de muertes al año, en todo el mundo. Además, este patógeno presenta la capacidad de infectar ciertas células del sistema inmunitario, como los monocitos, los macrófagos y las células dendríticas. Ello transforma a los inmunocitos en reservorios del microbio, hecho que favorece la diseminación y cronificación de la infección, a la vez que dificulta su tratamiento.
Ahora, investigadores del Instituto de Bioingeniería de Cataluña, liderados por Giuseppe Battaglia y Loris Rizzello, proponen el uso de nanovesículas artificiales, o polimerosomas, para mejorar la eficacia de los antibióticos. La revista ACS Nano publica el artículo en el que también participaron científicos de otros centros de investigación y universidades españoles e ingleses.
«Aunque no ocupe muchos titulares, aún nos hallamos lejos de erradicar la tuberculosis, responsable de la muerte de 3 personas cada minuto», declara, a Investigación y Ciencia, Loris Rizzello. «De hecho, la Organización Mundial de la Salud clasifica la tuberculosis dentro de las 10 principales causas de defunción en el mundo. Ello nos llevó a buscar estrategias terapéuticas para combatirla. En tiempo reciente, presentamos el resultado de 7 años de trabajo».
Una combinación de dos polímeros
Para encapsular y transportar hasta los macrófagos infectados los fármacos antibióticos, los autores diseñaron vesículas formadas por los polímeros poli-2-metacriloiloxi-etil fosforilcolina y poli-2-diisopropilamino metacrilato de etilo (PMPC y PDPA, por sus siglas en inglés, respectivamente). «La combinación PMPC-PDPA ofrece múltiples ventajas. Por un lado, el PMPC presenta una alta afinidad por los macrófagos, esencial para el éxito del sistema, ya que la Mycobacterium tuberculosis se esconde en estas células. Y por el otro, la sensibilidad a cambios de pH del PDPA permite mantener la estabilidad del antibiótico durante el transporte por el organismo; pero una vez dentro de la célula, el pH ligeramente ácido del entorno provoca la lenta liberación del fármaco», explica el investigador.
Experimentos realizados in vitro demostraron la estabilidad de los polimersomas de PMPC-PDPA, pues perduraron en solución acuosa durante más de un año. Asimismo, las vesículas resultaron biocompatibles y seguras, pues no provocaron la muerte de los macrófagos en cultivo, como tampoco indujeron la activación de la respuesta inflamatoria o la secreción de especies radicales de oxígeno.
Eliminar una bacteria mortal
«Trabajar con embriones de pez cebra resultó muy gratificante. Los modificamos genéticamente con el objetivo de marcar distintas células con proteínas fluorescentes. Ello, junto con su característica transparencia, nos permitió observar la distribución de los polimersomas por todo el organismo», relata Rizzello. «En ratones, es mucho más difícil establecer con precisión el destino final de las vesículas, pero queremos comparar ambos modelos. Si hallamos los mismos patrones de biodistribución, podremos concluir que el pez cebra constituye un sistema apto y válido para continuar futuros estudios».
En el presente estudio, los peces infectados por Mycobacterium marinum, el patógeno causante de la tuberculosis en los ectotermos, recibieron el antibiótico rifampicina encapsulado, por vía intravenosa. «Diez minutos después de la inyección, hallamos los polimersomas dentro de los macrófagos. En concreto, en el interior de los lisosomas, los orgánulos celulares que se encargan de la digestión celular, donde también se acumulan las bacterias. La localización en el mismo compartimento aumenta la efectividad del tratamiento», comenta el autor. «Esta es una de las grandes ventajas de las vesículas. Encapsular el fármaco evita que altere tejidos no afectados por la infección, y por consiguiente la aparición de efectos secundarios, a la vez que aumenta la concentración del compuesto en el interior celular».
Normalmente, las bacterias adquieren resistencia porque la dosis antibiótica no alcanza los valores mínimos necesarios para ocasionar su muerte. En consecuencia, algunas de ellas sobreviven y acaban por desarrollar tolerancia a los medicamentos. «Con los polimersomas ello no ocurre. La alta concentración intracelular de los antibióticos extermina las bacterias y evita la aparición de resistencia», señala Rizzello.
La acumulación de cientos de macrófagos, en estructuras conocidas como granulomas, constituye una característica de la tuberculosis. Por lo general, los fármacos no alcanzan dichos cúmulos, hecho que facilita la supervivencia de las bacterias. No obstante, los polimersomas sí lograron penetrar la masa esférica de inmunocitos y erradicar a los patógenos.
Las vesículas también resultaron efectivas para transportar otros antibióticos y combatir infecciones causadas por Mycobacterium bovis, y Staphylococcus aureus. Por lo que Rizzello y sus colaboradores esperan que su hallazgo contribuya no solo a luchar contra la tuberculosis, sino también contra la resistencia a los antibióticos.
Marta Pulido Salgado
Referencia: «Polymersomes Eradicating Intracellular Bacteria», de F. Fenaroli et al., en ACS Nano, publicado el 9 de junio de 2020.